Đề xuất cấp giấy đăng ký lưu hành 3 thuốc điều trị COVID-19 sản xuất tại Việt Nam
Tại cuộc họp chiều 5/1, Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế đồng ý đề xuất Bộ Y tế cấp giấy đăng ký lưu hành có điều kiện cho 03 thuốc chứa hoạt chất Molnupiravir có chỉ định điều trị COVID-19 của các cơ sở sản xuất trong nước.
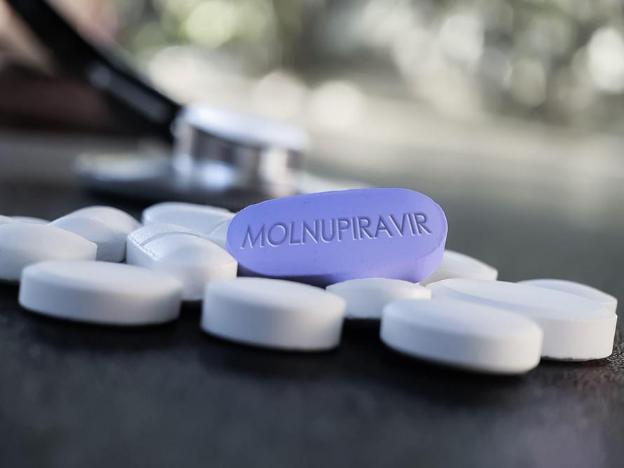 |
Tối 5/1, Bộ Y tế đã có thông tin về Phiên họp Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế về hồ sơ đăng ký lưu hành thuốc Molnupiravir.
Ngày 30/12/2021, Ủy ban Thường vụ Quốc hội ban hành Nghị quyết số 12/2021/UBTVQH15 về việc cho phép thực hiện một số cơ chế, chính sách trong lĩnh vực y tế để phục vụ công tác phòng, chống dịch COVID-19.
Trong đó, Ủy ban Thường vụ Quốc hội đã thống nhất quyết nghị cơ chế cấp phép thuốc mới có chỉ định sử dụng phòng, điều trị COVID-19 sản xuất trong nước có cùng hoạt chất, dạng bào chế, đường dùng với thuốc đã được cấp phép bởi cơ quan quản lý dược chặt chẽ (SRA) theo phân loại của Tổ chức y tế thế giới.
Căn cứ cơ chế cấp phép thuốc mới có chỉ định sử dụng phòng, điều trị COVID-19 tại Nghị quyết số 12/2021/UBTVQH15, Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế đã khẩn trương tổ chức phiên họp ngày 5/1/2022 để xem xét hồ sơ đề nghị cấp giấy đăng ký lưu hành thuốc chứa hoạt chất Molnupiravir của các cơ sở sản xuất trong nước.
Tại phiên họp, Hội đồng đã xem xét một cách kỹ lưỡng, thận trọng các ý kiến thẩm định của các tiểu ban chuyên môn, các chuyên gia đầu ngành về tiêu chuẩn chất lượng, bào chế, dược lý lâm sàng và thống nhất kết luận đồng ý đề xuất Bộ Y tế cấp giấy đăng ký lưu hành có điều kiện cho 3 thuốc chứa hoạt chất Molnupiravir có chỉ định điều trị COVID-19.
Các điều kiện cụ thể để kiểm soát chặt chẽ chất lượng thuốc sau khi được cấp giấy đăng ký lưu hành được Hội đồng yêu cầu đối với cơ sở sản xuất thuốc như sau:
Cơ sở sản xuất thuốc phải thực hiện kiểm tra chất lượng nguyên liệu đạt yêu cầu trước khi sản xuất;
Cơ sở sản xuất thuốc phải tiếp tục theo dõi, kiểm tra chất lượng thuốc hàng tháng sau khi được cấp giấy đăng ký lưu hành và báo cáo cơ quan quản lý để giám sát chặt chẽ về chất lượng, tuổi thọ của thuốc;
Cơ sở sản xuất phải thuốc phải tiếp tục thực hiện nghiên cứu độ ổn định của thuốc và nộp dữ liệu nghiên cứu, hồ sơ cập nhật hạn dùng để thẩm định theo hướng dẫn và yêu cầu của Bộ hồ sơ kỹ thuật chung ASEAN.
Đối với các hồ sơ chưa được phê duyệt, Hội đồng đề nghị các cơ sở sản xuất tiếp tục khẩn trương nghiên cứu, bổ sung các tài liệu, dữ liệu và kết quả nghiên cứu về tiêu chuẩn chất lượng thuốc, độ ổn định của thuốc. Hội đồng sẽ khẩn trương họp để xem xét việc cấp phép ngay khi có các kết quả thẩm định hồ sơ bổ sung của các tiểu ban chuyên môn.
Đối với việc cấp phép lưu hành thuốc điều trị COVID-19, Bộ trưởng Bộ Y tế yêu cầu các cơ quan quản lý và đơn vị chuyên môn kiểm soát chặt chẽ về chất lượng và quản lý về giá theo đúng quy định của Luật Dược, chống mọi biểu hiện tiêu cực, lợi ích nhóm trong việc cung ứng thuốc.
* Liên quan đến thuốc Molnupiravir, báo Sức khỏe và đời sống cho biết, đến nay, Bộ Y tế đã phân bổ hơn 300.000 liều cho 51 địa phương đang triển khai Chương trình sử dụng thuốc có kiểm soát cho F0 mắc COVID-19 thể nhẹ tại cộng đồng.
Trước đó, căn cứ kết quả đánh giá giữa kỳ của các nghiên cứu thử nghiệm lâm sàng tiến hành tại Bệnh viện Thống Nhất, Bệnh viện Phổi Trung ương, Đại học Y Dược TP HCM cho thấy tính an toàn và hiệu quả thuốc Molnupiravir, Bộ Y tế đã cho phép triển khai Chương trình sử dụng thuốc có kiểm soát Molnupiravir cho các trường hợp mắc COVID-19 thể nhẹ tại cộng đồng tại TP HCM từ giữa tháng 8/2021.
Các kết quả báo cáo giữa kỳ của chương trình tại 22 tỉnh/thành phố cho thấy thuốc Molnupiravir có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị với tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 5 ngày âm tính hoặc dương tính với giá trị CT ≥ 30 từ 72,1% đến 99,1%; tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 14 ngày âm tính hoặc dương tính với giá trị CT ≥ 30 gần 100%; tỷ lệ chuyển nặng rất thấp từ 0,02%-0,06% và không có ca nào dẫn đến tử vong./.
Cổng Thông tin điện tử Chính phủ
Bài viết cùng chuyên mục
Đọc thêm

Gia tăng cận thị học đường – Can thiệp sớm để bảo vệ đôi mắt trẻ
Hiện nay, tình trạng cận thị ở trẻ em đang gia tăng nhanh chóng, trở thành mối quan tâm của nhiều phụ huynh. Nếu không được phát hiện sớm và can thiệp kịp thời, cận thị có thể ảnh hưởng lâu dài đến thị lực và quá trình học tập của trẻ.

Bộ Y tế thông tin về biến thể SARS-CoV-2
Bộ Y tế vừa thông tin về biến thể mới của virus SARS-CoV-2 BA.3.2. Biến thể này được Tổ chức Y tế Thế giới WHO xếp vào nhóm biến thể đang theo dõi.

Bộ Y tế yêu cầu siết chặt điều trị và kiểm soát lây nhiễm bệnh tay chân miệng
3 tháng đầu năm 2026, cả nước ghi nhận hơn 25.000 ca tay chân miệng, tăng gấp 5 lần cùng kỳ, trong đó có 4 trường hợp tử vong. Bộ Y tế yêu cầu các cơ sở y tế tăng cường điều trị, kiểm soát lây nhiễm.

Ca mắc tay chân miệng tăng gấp 5 lần, 92% tập trung ở trẻ mầm non
Chỉ trong gần 3 tháng đầu năm 2026, cả nước ghi nhận hơn 25.000 ca tay chân miệng, tăng gấp 5 lần so với cùng kỳ năm trước. Đáng chú ý, bệnh chủ yếu xảy ra ở trẻ dưới 10 tuổi (chiếm 99,3%), trong đó nhóm từ 1 - 5 tuổi chiếm tới 92,7%.

Hiện đại hóa quy trình xử lý rác thải y tế
Nhằm giảm thiểu ô nhiễm môi trường và bảo vệ sức khỏe cộng đồng, ngành Y tế tỉnh Thanh Hóa đã triển khai các dự án hiện đại hóa quy trình xử lý chất thải. Trọng tâm là áp dụng mô hình xử lý theo cụm, sử dụng công nghệ tiệt trùng kết hợp cắt nghiền tiên tiến. Giải pháp này thay thế hoàn toàn phương pháp lò đốt thủ công và chôn lấp thông thường; giúp kiểm soát chặt chẽ nguy cơ lây nhiễm, bảo vệ môi trường.
Trạm y tế sẵn sàng chuyển đổi vận hành theo mô hình mới
Dự kiến, từ ngày 1/4/2026, các trạm y tế xã, phường tại Thanh Hóa sẽ chuyển đổi hoạt động theo mô hình mới, trực thuộc UBND cấp xã, phường quản lý thay vì Trung tâm y tế. Mô hình này giúp rút ngắn khoảng cách quản lý, tăng tính chủ động, bám sát nhu cầu y tế cơ sở và nâng cao hiệu quả chăm sóc sức khỏe Nhân dân.
Tỷ lệ đột quỵ ở Việt Nam thuộc nhóm cao nhất thế giới
Bộ Y tế ghi nhận Việt Nam hiện trong nhóm quốc gia có tỷ lệ đột quỵ cao, với 222.000 ca mỗi năm, song phần lớn chưa tiếp cận kịp thời hệ thống cấp cứu.

Cảnh báo thuốc giả dự phòng trước phơi nhiễm HIV
Cục Quản lý Dược (Bộ Y tế) vừa phát đi cảnh báo về sản phẩm thuốc tiêm YEZTUGO, hiện chưa được cấp phép tại Việt Nam nhưng đã xuất hiện dấu hiệu lưu hành trái phép trên thị trường. Đây là thuốc liên quan đến dự phòng trước phơi nhiễm HIV, nên việc sử dụng sản phẩm không rõ nguồn gốc có thể gây hậu quả nghiêm trọng.
Biến chứng võng mạc do đái tháo đường có thể gây mù lòa
Theo các chuyên gia y tế, đái tháo đường được ví như “kẻ cướp ánh sáng” thầm lặng khi có thể gây mù lòa nếu không được phát hiện và kiểm soát kịp thời.

Chủ động tiêm vaccine phòng bệnh viêm màng não mô cầu từ cộng đồng
Từ đầu năm 2026 đến nay, bệnh viêm màng não do não mô cầu diễn biến phức tạp, ghi nhận nhiều ca mắc và tử vong tại một số địa phương. Tại Thanh Hóa, hiện chưa ghi nhận ca bệnh, tuy nhiên người dân đã chủ động phòng ngừa bằng cách tiêm vaccine.




Bình luận
Thông báo
Bạn đã gửi thành công.